Theo đó, 125 thuốc sản xuất trong nước được gia hạn giấy đăng ký lưu hành hiệu lực 5 năm, 9 thuốc sản xuất trong nước được gia hạn giấy đăng ký lưu hành hiệu lực 3 năm, một thuốc sản xuất trong nước được gia hạn đăng ký lưu hành đến 31/12/2025.
Cục Quản lý Dược (Bộ Y tế) yêu cầu cơ sở sản xuất và cơ sở đăng ký thuốc có trách nhiệm sản xuất thuốc theo đúng các hồ sơ, tài liệu đã đăng ký với Bộ Y tế và phải in số đăng ký được Bộ Y tế cấp lên nhãn thuốc.
Các cơ sở chỉ được sản xuất, đưa ra lưu hành các thuốc kiểm soát đặc biệt khi có giấy chứng nhận đủ điều kiện kinh doanh dược phạm vi kinh doanh thuốc phải kiểm soát đặc biệt phù hợp với phạm vi hoạt động của cơ sở đáp ứng quy định tại khoản 5 Điều 143 Nghị định số 54/2017/NĐ-CP ngày 08/5/2017 của Chính phủ quy định chi tiết một số điều và biện pháp thi hành Luật Dược.
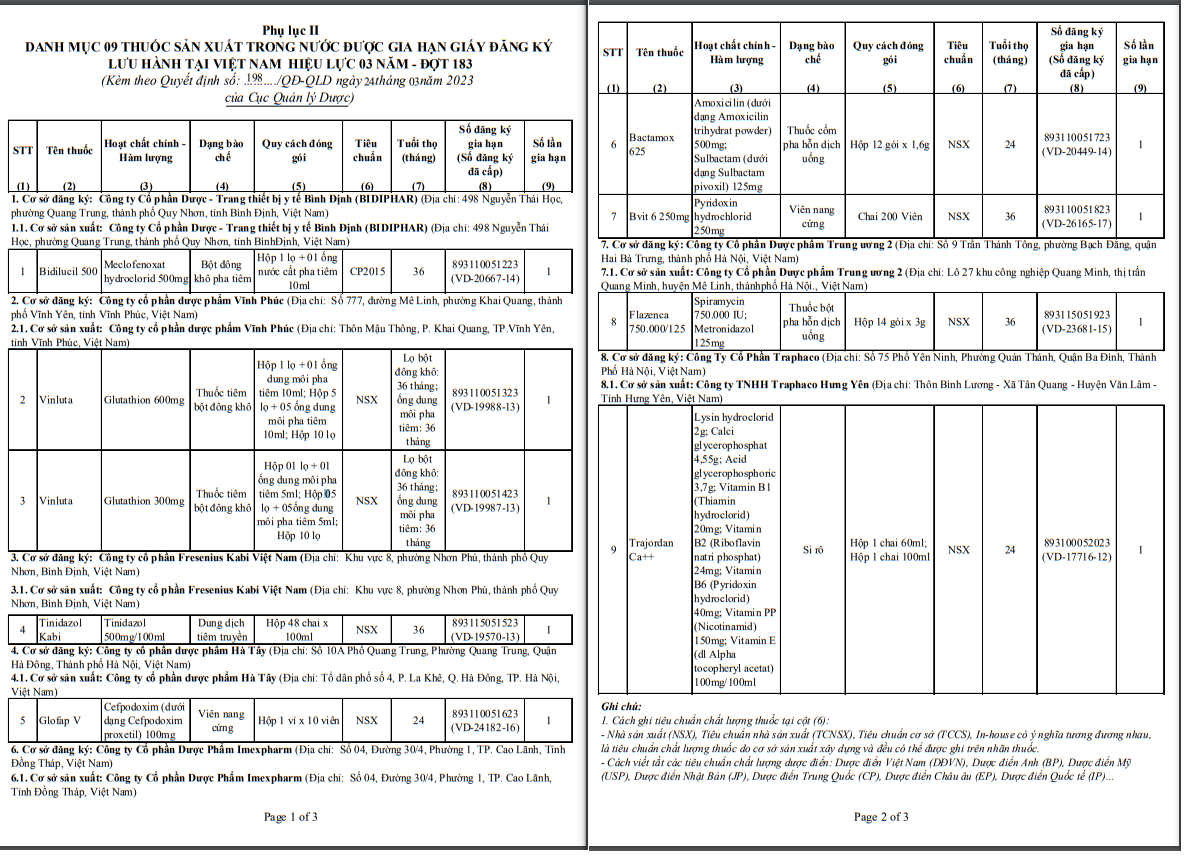
Danh mục 9 thuốc sản xuất trong nước được gia hạn giấy đăng ký lưu hành hiệu lực 3 năm.
Sau 12 tháng kể từ ngày ký ban hành quyết định trên, các thuốc được gia hạn giấy đăng ký lưu hành phải thay đổi về nội dung hành chính (bao gồm cả mẫu nhãn và tờ hướng dẫn sử dụng thuốc), sản xuất và lưu hành với các nội dung đã được phê duyệt thay đổi trong hồ sơ gia hạn.
Cơ sở đăng ký thuốc phải bảo đảm duy trì điều kiện hoạt động trong thời gian hiệu lực của giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc. Trong trường hợp không còn đáp ứng đủ điều kiện hoạt động, cơ sở đăng ký phải có trách nhiệm thực hiện thay đổi cơ sở đăng ký theo quy định tại Thông tư số 08/2022/TT-BYT trong thời hạn 30 ngày kể từ ngày cơ sở đăng ký không còn đủ điều kiện hoạt động.